全氟和多氟烷基物质(PFAS)由于其优异的工业特性,被广泛应用于多种工业产品和生活用品中。研究表明,以全氟辛基磺酸(PFOS)和全氟辛酸(PFOA)为代表的多种PFAS对机体的代谢、免疫、神经和胚胎发育等具有潜在的毒性影响。尽管一些PFAS在欧洲和北美已经被禁止生产和使用,但在部分亚洲地区,它们的产量及在环境中的检出水平呈上升趋势。PFAS可以在环境中持续存在,通过污染水和食物,经食物链进入机体内。即使接触水平较低,长期暴露也可能带来潜在的健康风险。既往流行病学研究和本团队基于上海优生儿童队列的前期研究发现,PFAS(尤其PFOS)暴露可增加妊娠期糖尿病的风险,引起糖代谢平衡紊乱,但其具体的代谢毒性机制并不十分清楚。尽管动物和细胞实验也提示高浓度的PFAS会导致高血糖症和胰岛素抵抗。由于既往不同动物和细胞研究中暴露剂量的差异,暴露剂量往往远高于人群实际接触剂量,使得研究观察到的代谢表型变化存在一定差异。不同剂量的PFAS暴露引起的器官毒性和涉及的毒性途径可能并不完全相同。因此,需要开展基于环境暴露水平阈剂量相关的机制研究,评估PFAS暴露的代谢毒性机制。
为此,上海交通大学医学院附属新华医院环境与儿童健康教育部与上海市重点实验室张军教授团队在Environment International(环境健康领域国际顶级学术期刊,IF=13.352,中科院一区)上,在线发表了题为“Metabolic perturbations in pregnant rats exposed to low-dose perfluorooctanesulfonic acid: An integrated multi-omics analysis”的研究论文,系统探讨了孕期低剂量PFOS暴露对孕晚期代谢稳态的影响。

一、研究方法
通过对SD孕鼠进行PFOS梯度染毒(0,0.03,0.3mg∙kg-1,以体重计),于孕晚期对母鼠进行口服葡萄糖耐量试验(OGTT)和生化测试,以评估葡萄糖稳态和血脂水平。通过转录组测序与非靶向代谢组检测相结合,进一步确定母鼠肝脏中暴露引起的差异基因和差异代谢物,并确定它们与母鼠代谢表型的关联。
二、研究结果
结果显示,在0.03mg∙kg-1 PFOS暴露组的母鼠肝脏中发现396个差异表达基因,包括203个上调基因和193个下调基因;在0.3mg∙kg-1 PFOS暴露组中发现529个差异表达基因,包括288个上调基因和241个下调基因(图1A和1B)。针对母鼠肝脏的UPLC-MS非靶向代谢组学检测,共匹配和识别3350个离子。结果提示,在负离子模式下,0.03 和0.3mg∙kg-1 PFOS暴露组分别发现164和158种代谢物。在正离子模式下,0.03 和0.3mg∙kg-1 PFOS暴露组分别发现104和56种差异代谢物(图1C和1D)。
▼图1 母鼠肝脏的转录组和代谢组火山图分析
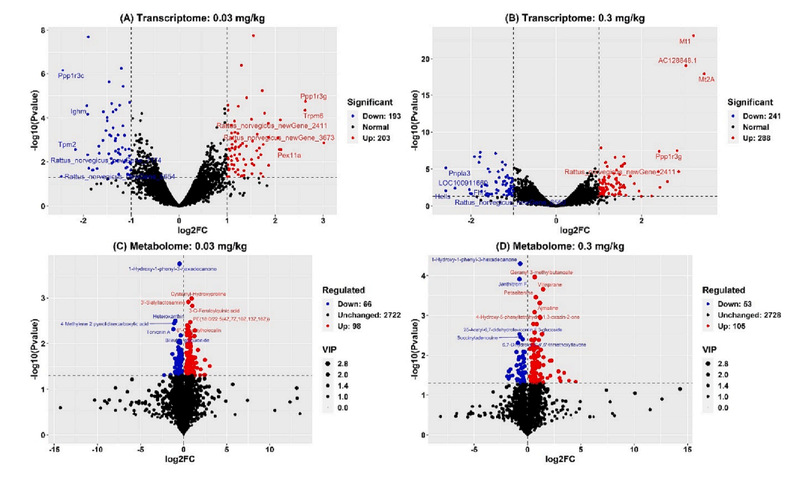
转录组差异基因的KEGG通路径富集分析显示,0.03mg∙kg-1的PFOS暴露可引起若干信号通路的变化,如类固醇合成、PPAR信号通路、脂肪酸降解、卵巢类固醇合成、AMPK信号通路、花生四烯酸代谢、丁酸甲酯代谢、胰岛素抵抗、胆固醇代谢等(图2)。0.3mg∙kg-1 PFOS暴露组的差异基因则与亚油酸代谢、化学致癌、AMPK信号通路、青少年成熟期糖尿病、类固醇激素生物合成和胰岛素信号通路的显著变化有关。差异代谢物的KEGG富集分析显示,0.03mg∙kg-1 PFOS暴露诱发的差异代谢物主要富集在α-亚麻酸代谢、糖酵解/葡萄糖生成、嘌呤代谢和胰高血糖素信号通路、半胱氨酸和蛋氨酸代谢、类固醇生物合成等(图2)。相应地,0.3mg∙kg-1 PFOS暴露引起的代谢物差异可能富集在甘氨酸、丝氨酸和苏氨酸代谢、亚油酸代谢、类固醇生物合成、肝细胞癌等方面。
▼图2 差异基因和差异代谢物的KEGG通路富集分析
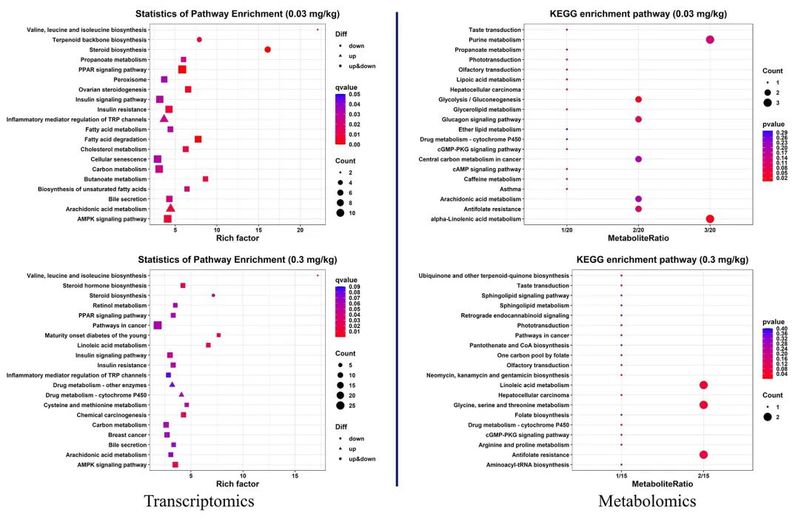
KEGG共同富集分析观察到若干个显著富集的途径,如花生四烯酸代谢、胆汁分泌、碳代谢、cGMP-PKG信号通路、果糖和甘露糖代谢、代谢中的甘油脂代谢,以及代谢组中的α-亚麻酸代谢和糖酵解/葡萄糖生成。其中,0.3mg∙kg-1 PFOS暴露组中,亚油酸代谢、甘氨酸、丝氨酸和苏氨酸代谢、类固醇生物合成途径和肝细胞癌途径的转录和代谢均发生了显著改变(P<0.05)(图3)。差异基因和代谢物与空腹血糖水平密切相关(图3)。对于0.03mg∙kg-1 PFOS暴露组,差异表达基因如Abcd2、Ogdh1、Ppp1r3g和差异代谢物如乳糖甘油酰胺、3-磷酸甘油和4-羟基-5-(苯基)-戊酸-O-葡萄糖醛酸与FBG水平密切相关。差异基因可富集于过氧化物酶体、碳代谢和胰岛素信号传导途径中。同样,对于0.3mg∙kg-1 PFOS暴露组,差异表达的基因和代谢物主要与FBG水平有关,Cyp2c23、Foxa3、Ppp1r3c、Foxa3、Cyp7a1等差异基因可富集于亚油酸代谢、化学致癌、类固醇激素生物合成、青少年成熟期糖尿病、胰岛素信号通路和胰岛素抵抗通路。
▼图3 差异基因和差异代谢物的共富集分析,及其与代谢表型的关联
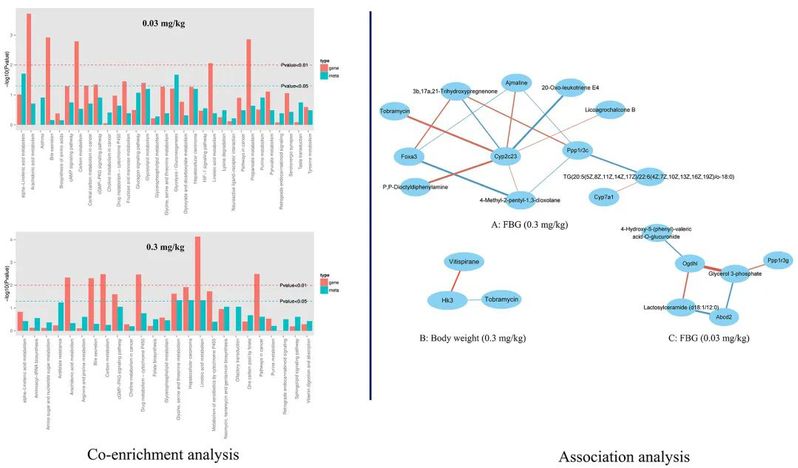
三、研究结论
本研究首次探索了较低浓度的PFOS暴露对怀孕大鼠肝脏转录组和代谢组的影响。我们发现,妊娠期PFOS暴露可引起一系列糖脂代谢相关途径中的基因表达和代谢物水平的变化。一些差异表达的基因如Abcd2、Ogdhl、Ppp1r3c和Ppp1r3g,以及代谢物如3-磷酸甘油和乳糖甘油酰胺可能在PFAS的代谢毒性中发挥重要作用。有必要对这些分子进行验证。
上海交通大学医学院附属新华临床医学院2019级博士研究生喻国旗(现新加坡国立大学杨潞龄医学院博士后)为该论文的第一作者,桂林医学院硕士研究生王巾帼为共同第一作者。研究得到了国家自然科学基金项目(81530086,41991314),上海市科学技术委员会项目(21410713500),上海市卫计委协同创新项目(2020CXJQ01)以及国家重点研发计划项目(2019YFA0802501)的大力支持。
供稿:上海优生儿童队列
原文链接:https://www.sciencedirect.com/science/article/pii/S0160412023001241?via%3Dihub